O Programa MDSAP – Medical Device Single Audit Program inciado em 2015 representa um aumento na segurança sanitária dos dispositivos médicos, uma vez que os organismos auditores inspecionam as empresas com maior frequência, atingindo em 2019 a marca de 5 mil empresas participantes, enviando relatórios anualmente para a Agência e para as demais autoridades que participam do programa. Além disso, 48,7% do total de Certificações Internacionais emitidas pela ANVISA para este setor foram feitas com a utilização do programa.
O MDSAP é racionaliza os recursos de inspeção na área de produtos de saúde, no qual, ao invés de várias autoridades sanitárias inspecionarem uma mesma planta de fábrica, uma única inspeção é realizada por um organismo auditor terceiro, que representa todas essas autoridades participantes do programa.
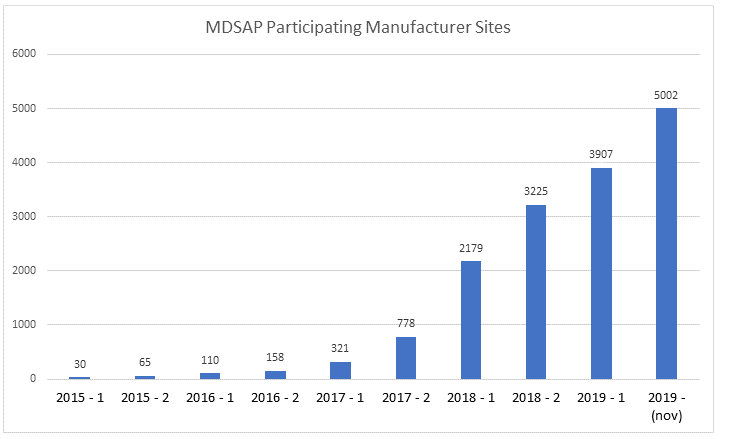
O programa teve início em 2015, com a participação de um pequeno número de empresas, até se consolidar como um programa de referência mundial em 2019, de acordo com o gráfico de evolução das empresas participantes do MDSAP abaixo:
 Fundação
Fundação
A Anvisa é membro fundadora do MDSAP, tendo desenhado e construído o programa desde o início, juntamente com as seguintes instituições: Therapeutic Goods Administration (TGA), da Austrália; Health Canada, do Canadá; U.S. Food and Drug Administration (FDA), dos Estados Unidos; Ministry of Health, Labour and Welfare (MHLW) e Pharmaceuticals and Medical Devices Agency (PMDA), do Japão.
Certificados emitidos
38 certificados emitidos pelo MDSAP em 2017 (4,7% do total).
107 certificados emitidos pelo MDSAP em 2018 (19,3% do total).
321 certificados emitidos pelo MDSAP em 2019 (48.7% do total).
Inspeções internacionais de produtos para a saúde
238 inspeções internacionais de produtos para a saúde (2017).
110 inspeções internacionais de produtos para a saúde (2018).
84 inspeções internacionais de produtos para a saúde (2019).
Saiba mais sobre o programa pelo link.



